Contexto:
El adenocarcinoma ductal de páncreas es un tipo de tumor que representa el 90% de los tumores malignos del páncreas. Se trata de un reto sanitario enorme, por varias causas. Por un lado, es uno de los tumores más agresivos y de progresión más rápida, lo que lleva al estremecedor dato de que el 95% de los pacientes fallecen. Por otro lado, generalmente se diagnostica tarde, y como además no hay tratamientos eficaces, la mortalidad es muy alta. Por estas razones, es el tercer tumor más mortal en España, pues se estima que en 2020 fallecerán 7120 pacientes por cáncer de páncreas.
Aunque los tratamientos contra el cáncer han evolucionado mucho durante los últimos años, los tratamientos que se usan de manera habitual contra el cáncer de páncreas siguen basándose en terapias con poca especificidad y considerables efectos secundarios.
Descripción del Proyecto:
Desde hace tiempo se sabe que la mayoría de los tumores de páncreas empiezan con mutaciones en una proteína que controla muchísimos procesos celulares, llamada K-Ras. Este es el primer paso de un proceso que continúa con acumulación de otras mutaciones que hacen que las células del páncreas se transformen en tumorales. Esto podría llevar a pensar que un tratamiento contra K-Ras podría ayudar a frenar el cáncer de páncreas, el problema es que, al menos hoy en día, no es posible atacar Ras mediante fármacos. No obstante, Ras dirige la función de otras proteínas, así que una estrategia factible sería dirigir los esfuerzos a bloquear a esas otras proteínas para impedir el desarrollo de los tumores.
Esto no es tan fácil como parece. Según esta hipótesis, habría que buscar tratamientos que ataquen proteínas que:
- Estén dirigidas y reguladas por Ras
- Si las eliminamos o desconectamos los tumores dejen de crecer
- Si las eliminamos o desconectamos las células sanas sobrevivan
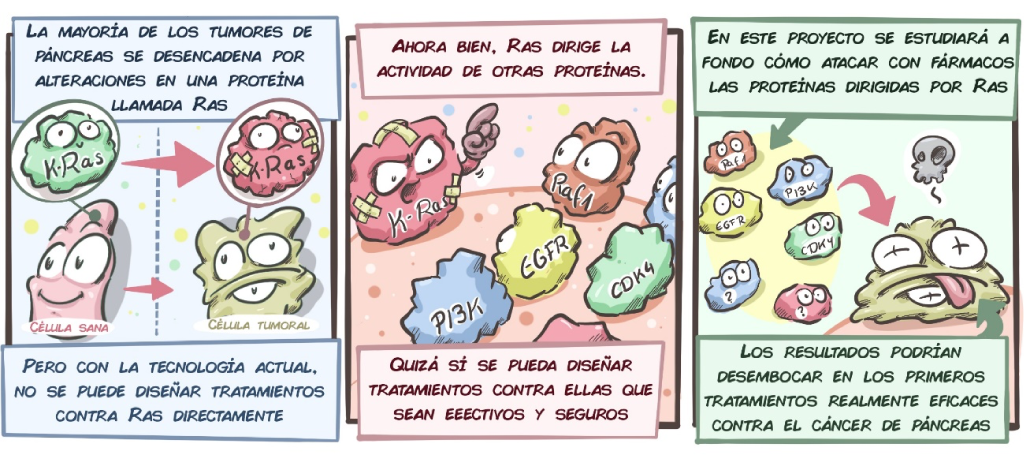
Después de años de intenso trabajo, el grupo del Dr. Barbacid encontró dos proteínas que cumplen estos criterios: Raf1 y EGFR. Pudieron comprobar en modelos de laboratorio que si se elimina simultáneamente estas proteínas la mitad de los tumores de páncreas dejaban de prosperar.
Estos fantásticos resultados son esperanzadores, ya que sugieren que los tratamientos contra EGFR y Raf1 podrían ser efectivos para los pacientes con cáncer de páncreas. Pero a su vez abren una serie de preguntas. En primer lugar, una proteína puede ser importante por su sola presencia (ya que puede hacer de soporte a otros elementos celulares) o por su actividad (al modificar a otros elementos celulares) ¿Los tumores sin Raf1 y EGFR se reducen porque estas proteínas no están, o porque no están activas? Es una diferencia sutil pero importante: Apagar la actividad de una proteína es relativamente abordable, pero destruirla mediante fármacos es más complicado (aunque posible).
Otra pregunta que surge es si hay otras proteínas relacionadas con Ras que podrían ser atacadas mediante tratamientos. Finalmente, hemos dicho que, en modelos de laboratorio, eliminar EGFR y Raf1 es efectivo contra la mitad de los tumores. ¿Qué pasa con la otra mitad? ¿Qué proteínas se podrían atacar mediante fármacos?
Todas estas preguntas son las que busca responder el ambicioso proyecto apoyado por CRIS “Identificación y validación de nuevas dianas terapéuticas” del Dr. Barbacid.
Objetivos del proyecto:
- Comprobar en modelos de laboratorio qué es lo que está causando la desaparición de los tumores cuando se elimina EGFR y Raf1 : ¿La eliminación completa? ¿O solamente la ausencia de su actividad?
- En el caso de que los tumores necesiten solamente la actividad de estas proteínas, se trabajará en el desarrollo de fármacos adecuados.
- En el caso de que los tumores requieran la presencia completa de la proteína, se trabajará en estrategias terapéuticas para degradar específicamente estas proteínas en los tumores de los pacientes.
- En paralelo se hará un estudio similar con otras proteínas que están controladas por Ras. Se hará hincapié en unas proteínas denominadas PI3K y CDK4.
- Finalmente, en los tumores que crecen incluso en ausencia de EGFR y RAF1 harán un screening en busca de nuevas dianas que se puedan tratar.
En resumen, se trata de un proyecto de gran alcance, que puede significar una de las apuestas más importantes para encontrar nuevas terapias para un tipo de cáncer que hoy en día tiene un enorme impacto sobre los pacientes.
¿Quiéres apoyar la investigación contra el cáncer de páncreas?
Haz tu donación y colabora para que podamos seguir luchando para acabar con el cáncer de páncreas
Dona ahoraÚltimos Avances:
El proyecto marcha a toda velocidad y cumpliendo sus objetivos puntualmente. Además, han realizado varios hallazgos muy relevantes en el campo del cáncer de páncreas.
Comprobación en modelos de laboratorio de los efectos de eliminar Raf1y EGFR:
El equipo del Dr. Barbacid ha conseguido responder a una de las principales preguntas de este proyecto: Cuando eliminaban EGFR y RAF1 en modelos animales, la mitad de los tumores de páncreas desaparecían, pero la duda consiste en si se debe a que la proteína no puede realizar sus funciones o porque directamente no está en absoluto. Esta cuestión es muy relevante: Farmacológicamente es mucho más sencillo bloquear la actividad de una proteína que eliminarla por completo.
En el caso de RAF1, los estudios han mostrado que no es suficiente con bloquear la actividad de RAF-1 para conseguir los efectos antitumorales. Estos resultados son muy relevantes, ya que explican por qué hasta la fecha los fármacos contra la actividad de RAF-1 han fracasado en los ensayos clínicos. Estos resultados se publicaron en la prestigiosa revista internacional Cancer Cell.
Ocurre lo mismo con EGFR: Los tumores sólo dejan de desarrollarse si eliminamos EGFR, no si bloqueamos su actividad.
Los próximos pasos, de cara a diseñar terapias que puedan llegar a los pacientes, consiste en diseñar unos fármacos especiales (llamados degradadores) que no bloqueen, sino que destruyan las molécula de RAF-1 y EGFR.
Estudio de proteínas controladas por Ras, con especial hincapié en PI3K y CDK4.
Como decíamos en la introducción, Ras controla muchas maquinarias celulares diferentes. Otros de los mecanismos controlados por Ras son las proteínas PI3K y CDK4.
Entre los resultados que han logrado este año, los investigadores han demostrado en modelos de laboratorio que, si además de eliminar RAF cancelamos la actividad de CD4K, se detiene el crecimiento tumoral y muchos tumores desaparecen. No obstante, con los fármacos actualmente en circulación no se consigue eliminar completamente la actividad de CDK4, así que se requerirán nuevas alternativas.
Realizaron experimentos similares para cancelar la actividad de PI3K combinada con la eliminación de RAF1 o de EGFR. Se lograron muy buenos resultados a la hora de eliminar los tumores, pero se producía una toxicidad tan fuerte en los modelos animales que se descartó este enfoque como estrategia terapéutica. Estos resultados, de todas maneras, podrían explicar por qué muchos compuestos contra PI3K han fracasado en los ensayos clínicos.
Identificación de nuevas dianas terapéuticas en cáncer de páncreas
Cuando hablábamos de que la mitad de los tumores de páncreas mueren cuando se les elimina EGFR y Raf1, ¿qué ocurre con la otra mitad? ¿Cómo eliminarlos?
Para responder a esta pregunta, el laboratorio del Dr. Barbacid está tomando tumores que sí responden a esa eliminación y otros que no, y están realizando un exhaustivo análisis molecular para compararlos (con especial atención al ADN, del ARN , de las proteínas y de su actividad).
El objetivo de este enfoque es doble. El primero es poder predecir qué tumores van a beneficiarse de la eliminación de EGFR y de Raf1. El segundo, identificar mecanismos que podamos atacar en los tumores que no respondan a la eliminación de EGFR y RAF1.
Por el momento ya han encontrado varios mecanismos que caracterizan a los dos grupos de tumores, y están realizando varios estudios para validar estos resultados.
Uno de los mecanismos en los que están trabajando es el que desencadena una proteína llamada STAT3. En modelos celulares han podido demostrar que si se elimina completamente esta proteína, tanto los tumores que morían al eliminar EGFR+Raf1 como los que no, eran eliminados. Ahora bien, realizar esto en modelos animales o en personas, como hemos dicho, es complicado: No es fácil eliminar una proteína en un organismo completo. No obstante, han conseguido utilizar un fármaco degradador que consigue eliminar STAT3 y provoca la muerte de las células tumorales en modelos de laboratorio. En estos momentos se están preparando para realizar experimentos con animales con este fármaco, pero deben planificarse con sumo cuidado por el elevadísimo coste de este compuesto.
Finalmente, para poder probar todas las estrategias terapéuticas que surjan de este proyecto en células humanas, el equipo ha conseguido hacerse con una colección de muestras de tumores de páncreas humano. Estas muestras son particulares, porque son cultivos celulares en tres dimensiones, que reproducen en gran medida cómo es el tumor en el individuo que lo padecía. Esto los convierte en una plataforma extraordinaria para poder experimentar con los tratamientos que se vayan desarrollando.
En resumen, los resultados hasta el momento son excelentes, ya que muestran que existen opciones terapéuticas para lograr eliminar los tumores de páncreas. Los avances que está realizando este proyecto pueden tener un enorme impacto en la manera que tenemos de tratar estos tumores tan agresivos.













